Helicobacter pylori – ein nahezu ubiquitärer Infektionserreger
Forschungsbericht (importiert) 2004 - Max-Planck-Institut für Infektionsbiologie
Mehr als die Hälfte der Weltbevölkerung ist mit Helicobacter pylori, dem bakteriellen Erreger diverser Erkrankungen des Magens, infiziert. Die Ansteckung erfolgt meist im Kindesalter. Über Jahrzehnte der asymptomatischen Besiedlung hinweg treten später bei etwa 10 bis 20% der Infizierten ernsthafte Symptome auf, von der chronischen Gastritis bis hin zum Magengeschwür und Magenkarzinom. So beispielsweise in der Volksrepublik China, einem Land mit besonders hoher Durchseuchungsrate (ca. 90%), wo etwa alle 2 bis 3 Minuten ein Mensch den Folgen des H. pylori induzierten Magenkarzinoms erliegt. Aber nicht nur wegen seiner immensen - und vermutlich noch immer unterschätzten - medizinischen und sozioökonomischen Bedeutung, sondern auch als global verbreitetes und molekularbiologisch interessantes, trickreiches infektiöses Agens bildet H. pylori ein herausforderndes Studienobjekt für die infektionsbiologische Forschung. Viele unserer Arbeiten zur Verbreitung und molekularen Pathogenese des Erregers werfen ein Licht auf Vorgänge, die auch für andere Felder der modernen Infektionsforschung Geltung haben. Außerdem liefern unsere Arbeiten innovative Ansatzpunkte zur Infektionsbekämpfung und zur Vorbeugung der Entstehung von Magenkrebs.
Phylogeographie von H. pylori
Die Phylogeographie beschreibt die Evolution (Phylogenie) bezogen auf geographisch-verteilte Populationen. Bakterien wurden bisher nicht unter diesem Gesichtspunkt untersucht, obwohl geographische Unterschiede für die Erreger von Meningitis, Tuberkulose und Lepra sowie H. pylori bekannt sind. Basierend auf ersten Hinweisen mit wenigen Isolaten aus Europa und Asien, wurden in der Forschergruppe Achtman DNA-Sequenzen für mehrere Gene aus einer Vielzahl von Isolaten aus aller Welt bestimmt. In enger Zusammenarbeit mit Prof. Sebastian Suerbaum (Medizinische Hochschule Hannover) sowie zahlreichen Mikrobiologen und Gastroenterologen wurde eine Stammsammlung mit 1.050 Isolaten aus 53 Ländern und allen Kontinenten etabliert. Von diesen Isolaten wurden jeweils Segmente von sieben Genen sequenziert, deren Produkte am intermediären Metabolismus beteiligt sind. Diese Sequenzen mit einer Gesamtlänge von 3.500 Basenpaaren beinhalten ungefähr 1.500 polymorphe Stellen, die eine gute Basis für populationsgenetische Untersuchungen darstellen.
Um die Populationstruktur von H. pylori anhand solcher Sequenzen zu analysieren und um die moderne und historische Populationstruktur von rekombinationsaktiven Bakterien unterscheiden zu können, wurde ein bioinformatisches Programm, „Structure“ genannt, auf das spezifische Vorhaben angepasst. So wurden fünf urstämmige Bakterienpopulationen identifiziert, die wahrscheinlich in Afrika, dem Nahen Osten und Asien ihren Ursprung hatten. Einige H. pylori wurden geographisch derart isoliert vorgefunden, dass sie ihren Urahnen noch stark ähnelten, wie z.B. Isolate aus Ostasien. Kontakte zwischen Menschen aus verschiedenen Regionen führten aber auch zu Mischinfektionen mit H. pylori aus verschiedenen Quellen. Nachfolgende genetische Rekombination zwischen diesen Bakterien ergaben wiederum Mosaikgene, die Nukleotide aus verschiedenen Urpopulationen beinhalteten („Admixture“). Während in Afrika und Zentralasien immer noch Isolate vorgefunden werden, deren Nukleotide größtenteils aus einer Urpopulation stammen, ist in Europa die Admixture zwischen zwei dieser Urpopulationen so weit fortgeschritten, dass man alle modernen Isolate als Hybride betrachten muss. Die modernen Populationen wurden mit Namen versehen, die ihre jetzige Verteilung widerspiegeln: hpEastAsia, hpAsia2 (Zentralasien), hpAfrica1, hpAfrica2 und hpEurope.
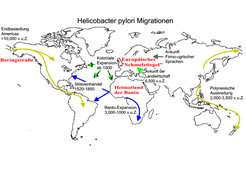
Historische Völkerwanderungen haben auch eine isolierte Entwicklung bestimmter H. pylori- Stämme begünstigt, was schließlich zur Separation von Subpopulationen führte. So entstand durch die Besiedlung Amerikas vor etwa 13.000 Jahren die Subpopulation hspAmerind; sie ist heute noch bei einigen Ureinwohnern Nord- und Südamerikas zu finden. Auf ähnliche Weise entstand die hspMaori- Subpopulation durch die pazifischen Seereisen der Polynäsier vor einigen Tausend Jahren. Auch diese Subpopulation kann noch heute in Maoris und Tongans in Neuseeland isoliert werden. Ebenso haben die Bantu-Migrationen von West- nach Süd-Afrika vor einigen Tausend Jahren zu einer Spaltung von hpAfrica1 in hspWAfrica und hspSAfrica geführt.
Migrationen aus noch jüngerer Zeit sind anhand der H. pylori-Sequenzen ebenfalls deutlich erkennbar. Isolate aus Nord- und Südamerika gehören zu hpEurope, wegen der europäischen Kolonisierung aber noch häufiger zu hpAfrica1, also H. pylori, die mit den Sklaven aus Afrika eingeführt wurden. Es ist auch leicht möglich, Isolate von Muslims und Buddhisten in Ladakh (Nordindien) zu unterscheiden. Ursprünglich trugen wahrscheinlich alle Einwohner Ladakhs hpAsia2-Isolate, aber die Einwanderung buddhistischer Schafhirten aus Tibet brachte zusätzlich zu der buddhistischen Religion auch so viele hpEastAsia H. pylori, dass alle modernen Isolate von Buddhisten nur ein Gemisch zwischen hpAsia2 und hpEastAsia darstellen. Umgekehrt scheint der Einstrom des Islams nicht über eine große Zahl muslimischer Missionare aus Saudi-Arabien (hpEurope) vollzogen worden zu sein, da nur drei Isolate von Muslimen hpEurope zugeordnet werden konnten und der Rest reine hpAsia2 darstellte. Auf der Basis dieser Beobachtungen werden jetzt Isolate verschiedener Urvölker mit dem Ziel untersucht, weitere Einsichten in humane Migrationen zu erhalten (Abb. 1).
Eindrucksvoll ist, wie präzise sich geschichtliche Ereignisse in der Populationsstruktur von H. pylori abgebildet haben. Ein wichtiges Element dieses historischen ‚Imprintings’ beruht auf dem effizienten Vollzug eines Genaustauschs zwischen unterschiedlichen H. pylori-Stämmen. Es wird angenommen, dass bei diesem Prozess die natürliche Transformierbarkeit der Erreger, also die Fähigkeit, nackte DNA zwischen Bakterien zu übertragen, eine entscheidende Rolle spielt. Unsere neusten molekulargenetischen Befunde, die wir kürzlich zusammen mit Dr. Steffen Backert, Magdeburg, erhalten haben, legen allerdings nahe, dass neben DNA-Transformation spezielle konjugative Prozesse eine zentrale Rolle beim horizontalen Genaustausch von H. pylori spielen könnten.
Molekularbiologie der H. pylori-Wirtszell-Interaktion
H. pylori hat einzigartige Mechanismen entwickelt, im feindlichen Milieu des Magens zu überleben. Charakteristisch für den menschlichen Magen ist die Ausbildung einer dichten Schleimschicht, welche die mukosale Epithelzelloberfläche vor dem Angriff der Magensäure schützt. In dieser Schleimschicht, die der Erreger mittels seiner ‚motorisierten’ Flagellen durchdringt, aber auch in direktem Kontakt mit den Epithelzellen hält sich H. pylori vorzugsweise auf. Ein wichtiges Enzym des Erregers ist die Urease, die verfügbaren Harnstoff spaltet und durch die Bildung von Ammoniak ein neutrales Mikromilieu erzeugt. Die Pathologie der Infektion hingegen wird weitgehend durch die direkte Wechselwirkung mit dem Magenepithel bestimmt. Es ist daher ein besonderes Anliegen, diese Interaktion der Bakterien mit den Wirtszellen genau zu untersuchen.
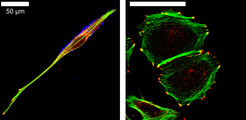
Die Mehrzahl aller schweren Infektionen, die mit Ulzerationen des Magens oder Zwölffingerdarms, dem MALT- („mucosa associated lymphoid tissue“) Lymphom oder dem Magenkarzinom einhergehen, wird durch so genannte Typ-I H. pylori Stämme hervorgerufen. Typ-I-Stämme unterscheiden sich von den vermutlich harmloseren Typ-II-Stämmen durch Gegenwart eines 40 kb langen Gensegments, der Zytotoxin-assoziierten Pathogenitätsinsel (CagPAI), die ein Typ-IV-Sekretionssystem kodiert. Wir konnten zeigen, dass ein bakterielles Protein, CagA, mithilfe dieses Sekretionsystems über einen noch wenig verstandenen Prozess in die Wirtzellen injiziert wird. Sobald CagA in der Wirtszelle angelangt ist, wird es durch Kinasen der Src-Familie an einer definierten Stelle phosphoryliert. Dabei wird die Src-Kinase selbst inaktiviert, und in der Folge kommt es dann zur Dephosphorylierung verschiedener Wirtszellproteine, die mit dem Aktin-Zytoskelett in Verbindung stehen. Dies führt zu starken Veränderungen im Zytoskelett der Wirtszellen, die durch eine extreme Elongation der Zellen („Kolibri“-Phänotyp, Abb. 2) charakterisiert sind und schließlich zu einer Auflösung sowohl des Zellverbandes als auch der Zell-Matrix-Interaktion führen.
Auf molekularer Ebene stehen beide Effekte in direktem Zusammenhang mit der Injektion und Phosphorylierung von CagA. Besonders interessant ist allerdings die Beobachtung, dass der Verlust der Zell-Matrix-Interaktion eng mit der Dephosphorylierung eines der zellulären Proteine, dem Vinculin, in Verbindung steht. Schaltet man mit einem genetischen Trick (mittels RNA Interferenz) die Bildung von Vinculin aus und komplementiert die Zelle gleichzeitig mit einem spezifisch mutierten Vinculin, das sich nicht mehr phosphorylieren lässt, so bildet sich der Kolibri-Phänotyp bereits nach sehr kurzem Kontakt mit dem Erreger. In diesem Fall trat von vornherein ein Verlust der Bindung des Vinculins an den so genannten Arp2/3-Komplex auf, der für den Aufbau der fokalen Kontakte, den Bindungsstellen zur Zellmatrix, wichtig ist. Diese Untersuchungen ergeben Einblicke in die molekularen Prozesse, die mit großer Wahrscheinlichkeit der Pathogenese von H. pylori Infektionen zugrunde liegen.
Ein Impfstoff gegen H. pylori
Die zunehmende Resistenz von H. pylori gegen die in der Therapie angewendeten Antibiotika und die Tatsache, dass diese Therapie Neuinfektionen nicht verhindert, sind die Hauptgründe für die Entwicklung eines Impfstoffes. Im Tiermodell konnte gezeigt werden, dass eine Impfung sowohl als Prophylaxe wie auch als Therapie im Prinzip wirksam sein könnte. H. pylori kolonisiert die Magenschleimhaut; ein Impfstoff sollte also eine schützende, mukosale Immunantwort auslösen. Da sich Salmonellen besonders dafür eignen, eine humorale wie auch zelluläre mukosale Immunantwort zu induzieren, setzen wir auf die Entwicklung einer rekombinanten Lebendvakzine auf der Basis von abgeschwächten Salmonella-Impfstoffbakterien. Unsere Strategie hat vier Säulen: 1. Entwicklung geeigneter Impfstoffträger, d.h. Optimierung von Salmonellenstämmen für die Immunisierung. 2. Auswahl geeigneter Impfantigene von H. pylori. 3. Erforschung der Schutzwirkung mit dem Ziel, Impfstoffträger rational zu verbessern. 4. Durchführung klinischer Versuche, um die Wirksamkeit unseres Impfstoffes zu untersuchen.
Ein für die Anwendung beim Menschen geeigneter Impfstoffträger ist der gegen Typhus eingesetzte Lebendimpfstoff Salmonella enterica Serovar Typhi Ty21a, eine chemisch attenuierte Salmonelle. Für diesen Impfstoff entwickelten wir Plasmid-gestützte Expressionssysteme, um H. pylori-Antigene in immunogener Form zu exprimieren. Für die Immunreaktion sind die absolute Menge an H. pylori-Protein und der Zeitpunkt der Synthese der Impfantigene während der Impfung von entscheidender Bedeutung. Optimierte Expression konnten wir durch eine geeignete Kombination von Promotor und Translationseffizienz bereits erreichen.
Durch eine umfassende Charakterisierung der immunogenen Proteine von H. pylori konnten wir Kriterien ableiten, durch die sich Impfantigene mit hoher Wahrscheinlichkeit identifizieren lassen. Das von uns definierte Immunoproteom beschreibt mehr als 600 immunogene Molekülspezies. Diese Antigene wurden von Seren infizierter Patienten erkannt. Ein Vergleich mit dem gesamten Proteom ergab, dass immunogene Proteine vornehmlich solche sind, die in relativ hoher Kopienzahl von H. pylori synthetisiert werden. Geeignete Impfantigene sind deswegen vor allem in den häufig vorkommenden Proteinklassen zu finden, die auch in der natürlichen Infektion vom Immunsystem erkannt werden. H. pylori zeigt eine hohe genetische Variabilität und ein Impfstoff, der gegen alle H. pylori-Stämme wirken sollte, muss auf Impfantigene beruhen, die innerhalb der H. pylori-Stämme möglichst konserviert sind. Trotzdem sollte der Impfstoff spezifisch für H. pylori sein und ein Impfantigen deswegen nur wenige Homologien zu Proteinen anderer Erreger aufweisen. Die Kombination dieser Kriterien erlaubte nicht nur, alle bisher experimentell gefundenen Impfantigene ‚vorherzusagen’, sondern auch zwei völlig neue Antigene zu identifizieren. Diese konnten wir erfolgreich im Tierversuch als Impfstoffkandidaten bestätigen.
H. pylori ist ein humanspezifischer Krankheitserreger und entsprechend ist die Aussagekraft von Tiermodellen, insbesondere von Kleintiermodellen, unklar. Die Frage, ob eine Impfung auch beim Menschen wirken kann, ist unbeantwortet. Aus diesem Grund haben wir für die klinische Erprobung unseres Impfstoffes ein Studienprotokoll entwickelt, bei dem freiwillige Probanden geimpft und danach experimentell mit H. pylori infiziert werden. Die Infektion wird nach einer Beobachtungsphase durch eine Antibiotikatherapie beendet. Dieses Protokoll hat anderen Ansätzen gegenüber entscheidende Vorteile: Der verwendete H. pylori-Stamm wurde speziell für diesen Einsatz von unseren Kooperationspartnern in Houston entwickelt und ist zu 100% therapierbar. Im Unterschied zur Alternative einer therapeutischen Impfung bereits infizierter Patienten ist die Gefahr einer pathologischen Immunreaktion, wie sie in Patienten durch die chronische Infektion vorliegen kann, nicht vorhanden. Mit dem von uns entwickelten Studienprotokoll konnten wir sodann erstmals zeigen, dass ein humaner, rekombinanter Lebendimpfstoff tatsächlich wirksam sein könnte. In einer Phase-I-Studie konnte in drei von neun geimpften Probanden nach einer experimentellen Infektion H. pylori nicht mehr nachgewiesen werden, während alle Kontrollprobanden bis zur Beendigung der Studie und der Eradikation der Infektion mit Antibiotika infiziert blieben. Diese noch anfänglichen Studien lassen auf die Entwicklung eines wirksamen Impfstoffs hoffen, der nicht nur gegen die Infektion gerichtet, sondern auch nachhaltig gegen Magenkrebs schützen könnte.

